
Farmacovigilancia e Inteligencia Artificial: Revisión de Eventos Adversos en Literatura Médica
La farmacovigilancia es un proceso crítico en la industria farmacéutica que puede tener un papel fundamental en la salud de los pacientes y en los ingresos de la industria.

¿Qué resolvemos?
El enfoque tradicional en el proceso de detección de efectos adversos es un proceso manual que requiere de invertir en recursos humanos especializados para procesar y analizar múltiples fuentes de información; pero es costoso y muy limitado en términos de volumen, velocidad y profundidad.
¿Cómo lo resolvemos?
La Inteligencia Artificial Semántica puede potenciar la capacidad, la velocidad y la profundidad del procesamiento y el análisis de datos mediante una combinación de tecnologías de Procesamiento del Lenguaje Natural, Generación del Lenguaje Natural y Aprendizaje Automático.

Búsqueda, extracción y consolidación
– Búsquedas multi-idioma en diversas fuentes de literatura médica con frecuencias diarias, semanales, mensuales.
– Extracción e integración de los documentos que contengan posibles eventos adversos según los parámetros definidos por el usuario o el diccionario MeDRA.
– Consolidación de una cola de documentos para su revisión por un experto en farmacovigilancia con soporte de I.A.
Detección, clasificación y validación
– Detección de eventos adversos según los criterios mínimos (Paciente, Reporte, Evento, Producto) y otros criterios de consideración.
Aviso de ausencia de criterios
Aviso de evento de seguridad
Aviso de falla de calidad
– Evaluación de la seriedad o gravedad de acuerdo a la definición internacional o local.
– Evaluación de la casualidad del caso de acuerdo a algoritmos (Naranjo, Kahrl y Lasagna, OMS, FDA, egtc)
Seguimiento, documentación y registro
– Registro del caso incluyendo fecha de identificación, conceptos clave, activos, fuente, motivo de descarte, información de seguridad.
– Seguimiento del caso mediante creación de alertas por falta de requisitos para complementar un caso. Revisión de la coherencia de la base de datos para encontrar duplicados, pendientes e incompletos
– Exportación de casos en formato PDF o XLM según los requerimientos regulatorios.
¿Qué ofrecemos?
dezzai proporciona al cliente una plataforma modular para aumentar la capacidad de detección y análisis de eventos adversos relacionados con los medicamentos:

Smart connector
Extracción automatizada e integración de informes de eventos adversos desde múltiples canales (correo electrónico, informes médicos, centro de llamadas, programas de apoyo al paciente, etc.)

Smart validator
Clasificación y validación de eventos adversos o eventos relacionados con fallos de calidad utilizando un modelo de Procesamiento del Lenguaje Natural entrenado por un experto humano y siguiendo protocolos y estándares de la industria.
Smart validator
Clasificación y validación de eventos adversos o eventos relacionados con fallos de calidad utilizando un modelo de Procesamiento del Lenguaje Natural entrenado por un experto humano y siguiendo protocolos y estándares de la industria.


Smart alerts
Sistema de notificación automatizado basado en reglas para eventos adversos, requisitos incompletos o hallazgos.

Smart reports
Reportes o resúmenes de conclusiones para apoyar la creación de informes de cumplimiento.
Smart reports
Reportes o resúmenes de conclusiones para apoyar la creación de informes de cumplimiento.

Software flexible e intuitivo que cumple con las regulaciones de la industria
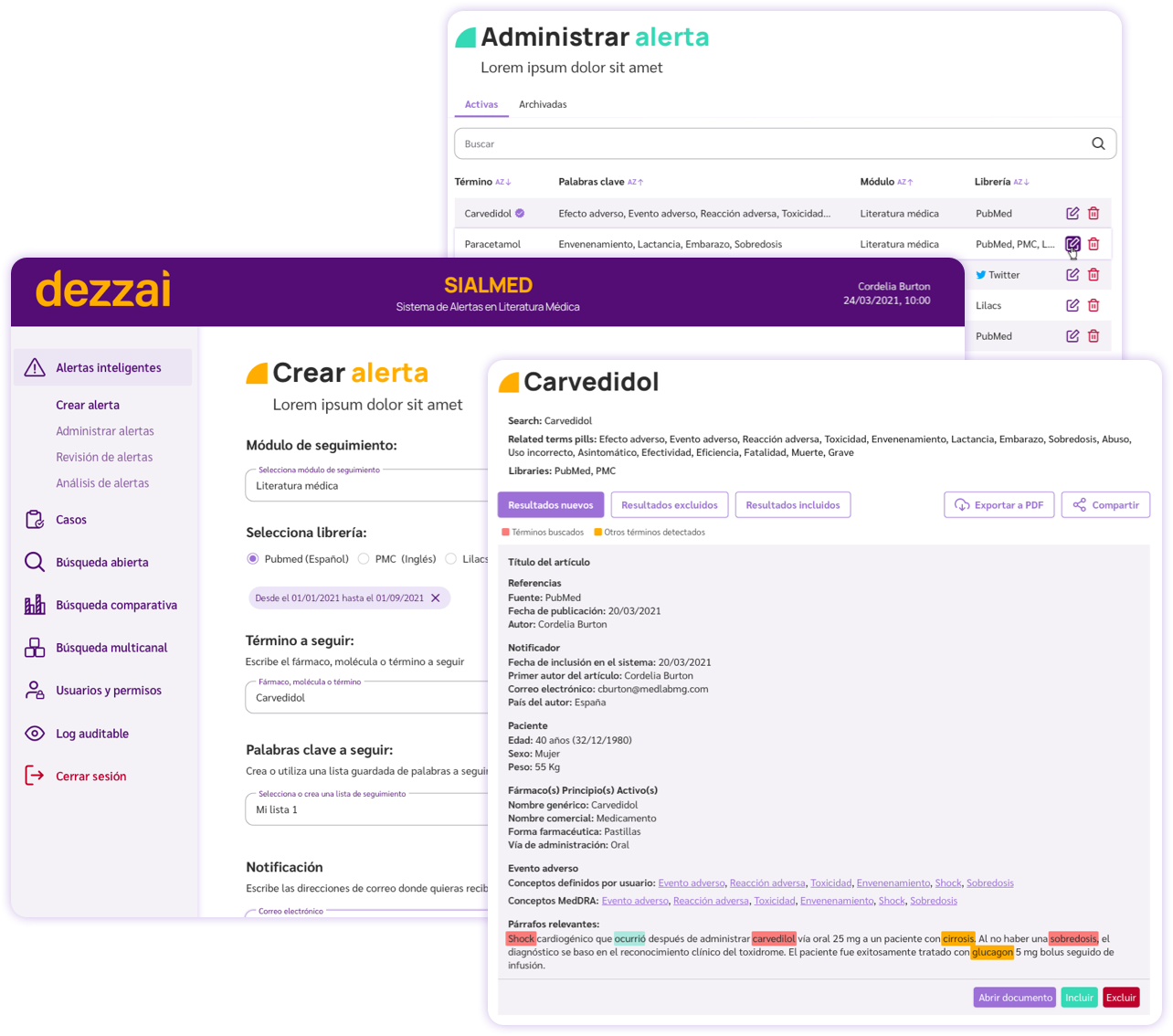
- ✅ Agilizar la búsqueda de posibles eventos adversos
- ✅ Facilitar la clasificación y valoración de eventos adversos mediante algoritmos de I.A. en conjunto con un experto en Farmacovigilancia
- ✅ Simplificar el seguimiento, registro y documentación de los eventos adversos
Descarga el folleto
Descárgate gratis nuestro folleto para tener más información sobre el caso de uso:
Otros casos de uso

Farmacovigilancia e IA – Gestión de casos

Redacción médica inteligente

Estudios observacionales y ensayos clínicos

Imagen médica

Análisis de texto médico
Estamos aquí para ayudarte
Certificada por:





